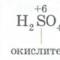Химические свойства. Химия Концентрированная азотная кислота
По химическому составу соли классифицируют на средние, кислые, основные и двойные .
Отдельным типом солей являются комплексные соли
(соли с комплексными катионами или анионами) . В формулах этих солей
комплексный ион заключён в квадратные скобки.
Комплексные ионы
- это сложные ионы, состоящие из ионов элемента (комплексообразователя)
и связанных с ним нескольких молекул или ионов (лигандов).
Примеры комплексных
солей приведены ниже.
а) С комплексным анионом:
K
2
[
PtC
l] 4
- тетрахлороплатинат(II
)
калия,
K
2
[
PtCl
] 6
- гексахлороплатинат(IV
)
калия,
К 3 [ Fe (CN ) 6 ] - гексацианоферрат(III ) калия.
Б) С комплексным катионом:
[ Cr (NH 3 ) 6 ] Cl 3 - хлорид гексаамминхрома (III ),
[
Ag
(NH
3
) 2 ]
Cl
- хлорид диамминсеребра (I
)
[Cu
(NH
3
) 4
]SO
4
-сульфат тетраамминмеди
(II
)
Растворимые соли при растворении в воде
диссоциируют на катионы металлов и анионы кислотных остатков.
NaCl → Na + +
Cl -
K 2 SO 4 → 2K +
+ SO 4 2-
Al(NO3)3 → Al 3+ + 3NO 3 -
1. Металл + неметалл = соль
2Fe
+ 3Cl
2
= 2FeCl
3
2. Металл + кислота = соль + водород
Zn
+ 2HCl
= ZnCl
2 + H
2
3. Металл + соль = другой металл + другая соль
Fe + CuSO 4 = Cu + FeSO 4
4. Кислота + основный (амфотерный) оксид = соль
+ вода
3H
2 SO
4 +Al
2 O
3 =Al
2 (SO
4) 3 +
3H
2 O
5. Кислота + основание = соль + вода
H
2 SO
4
+ 2NaOH
= Na
2 SO
4
+ 2H
2 O
При неполной нейтрализации многоосновной кислоты основанием
получают кислую соль
:
H
2 SO
4
+ NaOH
= NaHSO
4
+ H
2 O
При неполной нейтрализации многокислотного основания кислотой
получают основную соль
:
Zn
(OH
) 2
+ HCl
= ZnOHCl
+
H
2 O
6. Кислота + соль = другая кислота + другая соль
(для этой реакции используют более сильную кислоту)
AgNO 3 + HCl = AgCl + HNO 3
BaCl 2 + H 2 SO 4
= BaSO 4 + 2HCl
7. Основный (амфотерный) оксид + кислота = соль
+ вода
CaO + 2HCl = CaCl 2 +H 2 O
8. Основный оксид + кислотный оксид = соль
Li 2 O+CO 2 = Li 2 CO 3
9. Кислотный оксид + основание = соль + вода
SO3 + 2NaOH = Na 2 SO 4
+ H 2 O
10. Щёлочь + соль = основание + другая соль
CuSO
4 + 2NaOH
= Cu
(OH
) 2
+ Na
2 SO
4
11. Реакция обмена между солями: соль(1) + соль
(2) = соль(3) + соль(4)
NaCl + AgNO 3 =Na NO 3
+ AgCl
12. Кислые соли
могут быть получены
действием избытка кислоты на средние соли и оксиды:
Na
2 SO
4
+ H
2 SO
4
= 2NaHSO 4
Li
2O
+ 2H
2 SO
4
= 2LiHSO
4 + H 2 O
13. Основные соли
получают при осторожном
добавлении небольших количеств щелочей к растворам средних солей:
AlCl 3 + 2NaOH = Al(OH) 2 Cl +
2NaCl
1. Соль + щёлочь = другая соль + другое
основание
CuCl 2 + 2KOH = 2KCl + Cu(OH) 2
2. Соль + кислота = другая соль + другая кислота
BaCl
2 +
H
2 SO
4
= BaSO
4 + 2HCl
3. Соль(1) + соль (2) = Соль(3) + соль(4)
Na 2 SO 4 + BaCl 2
=2NaCl + BaSO 4
4. Соль + металл = другая соль + другой металл
(согласно электрохимическому ряду напряжений металлов)
Zn + Pb(NO 3) 2
= Pb + Zn(NO 3) 2
5. Некоторые соли разлагаются при нагревании
CaCO 3 = CaO + CO 2
KNO 3 = KNO 2
+ O 2
Специфические химические свойства солей зависят от того, какой катион и какой анион образуют данную соль.
|
Специфические свойства солей по катиону |
Специфические свойства солей по аниону |
|
Ag + + Cl - = AgCl ↓ белый творожистый осадок Cu 2+ + 2OH - = Cu (OH ) 2 ↓ синий осадок Ba 2+ + SO 4 2- = BaSO 4 ↓ белый мелкокристаллический осадок Fe 3+ + 3SCN - = Fe (SCN ) 3 кроваво-красное окрашивание Al 3+ + 3OH - = Al (OH ) 3 ↓ белый желеобразный осадок Ca 2+ + CO 3 2- = CaCO 3 ↓ белый осадок |
Ag + + Cl - = AgCl ↓ белый творожистый осадок Ba 2+ + SO 4 2- = BaSO 4 ↓ белый мелкокристаллический осадок 2H + + SO 3 2- = H 2 O + SO 2 газ с резким запахом 2H + + CO 3 2- = H 2 O + CO 2 газ без запаха 3Ag + + PO 4 3- = Ag 3 PO 4 ↓ жёлтый осадок 2H + + S 2- = H 2 S газ с неприятным запахом тухлых яиц |
Задание 1.
Из приведённого перечня выберите
соли, назовите их, определите тип.
1)
КNO 2
2)
LiOH 3) CaS 4) CuSO 4 5) P 2 O 5
6) Al(OH) 2 Cl 7) NaHSO 3 8) H 2 SO 4
Задание 2.
С какими из перечисленных веществ
может реагировать а) BaCl
2 б)
CuSO
4 в)
Na 2 CO 3 ?
1)Na 2 O 2)HCl 3)H 2 O 4) AgNO 3 5)HNO 3
6)Na 2 SO 4 7)BaCl 2 8)Fe
9)Cu(OH) 2 10) NaOH
С разбавленными кислотами, которые проявляют окислительные свойства за счет ионов водорода (разбавленные серная, фосфорная, сернистая, все бескислородные и органические кислоты и др.)
реагируют металлы:
расположенные в ряду напряжений до водорода
(эти металлы способны
вытеснять водород из кислоты);
образующие с этими кислотами растворимые соли
(на поверхности этих металлов
не образуется защитная солевая
пленка).
В результате реакции образуются растворимые соли
и выделяется водород:
2А1 + 6НСI = 2А1С1 3 + ЗН 2
М
g
+ Н 2
SO
4
=
М
gS
О 4
+ Н 2
разб.
С
u
+ Н 2
SO
4
→
X
(так
как С
u
стоит после Н 2)
разб.
РЬ + Н 2
SO
4
→
X
(так
как РЬ
SO
4
нерастворим
в воде)
разб.
Некоторые кислоты являются окислителями за счет элемента, образующего кислотный
остаток, К ним относятся концентрированная серная, а также азотная кислота
любой концентрации. Такие кислоты называют кислотами-окислителями.

Окислительные свойства кислотных остатков и значительно сильнее, чем нона водорода Н, поэтому азотная и концентрированная серная кислоты взаимодействуют практически со всеми металлами, расположенными в ряду напряжений как до водорода, так и после него, кроме золота и платины. Так как окислителями в этих случаях являются ноны кислотных остатков (за счет атомов серы и азота в высших степенях окисления), а не ноны водорода Н, то при взаимодействии азотной, а концентрированной серной кислот с металлами не выделяется водород. Металл под действием данных кислот окисляется до характерной (устойчивой) степени окисления и образует соль, а продукт восстановления кислоты зависит от активности металла и степени разбавления кислоты

Взаимодействие серной кислоты с металлами
Разбавленная и концентрированная серные кислоты ведут себя по-разному. Разбавленная серная кислота ведет себя, как обычная кислота. Активные металлы, стоящие в ряду напряжений левее водорода
Li, К , Ca, Na, Mg, Al, Mn, Zn, Fe, Co, Ni, Sn, Pb, H2, Cu, Hg, Ag, Au
вытесняют водород из разбавленной серной кислоты. Мы видим пузырьки водорода при добавлении разбавленной серной кислоты в пробирку с цинком.
H 2 SO 4 + Zn = Zn SO 4 + H 2
Медь стоит в ряду напряжений после водорода – поэтому разбавленная серная кислота не действует на медь. А в концентрированной серной кислоты, цинк и медь, ведут себя таким образом…
Цинк, как активный металл, может образовывать с концентрированной серной кислотой сернистый газ, элементарную серу, и даже сероводород.
2H 2 SO 4 + Zn = SO 2 +ZnSO 4 + 2H 2 O
Медь - менее активный металл. При взаимодействии с концентрированно серной кислотой восстанавливает ее до сернистого газа.
2H 2 SO 4 конц. + Cu = SO 2 + CuSO 4 + 2H 2 O
В пробирках с концентрированной серной кислотой выделяется сернистый газа.
Следует иметь в виду, что на схемах указаны продукты, содержание которых максимально среди возможных продуктов восстановления кислот.
На основании
приведенных схем составим уравнения конкретных реакций — взаимодействия меди и
магния с концентрированной серной кислотой:
0 +6
+2 +4
С
u
+ 2Н 2
SO
4
= С
uSO
4
+
SO
2
+ 2Н 2
O
конц.
0 +6 +2 -2
4М
g
+ 5Н 2
SO
4
= 4М
gSO
4
+ Н 2
S
+ 4Н 2
O
конц.
Некоторые металлы ( Fe . АI, С r ) не взаимодействуют с концентрированной серной и азотной кислотами при обычной температуре, так как происходит пассивации металла. Это явление связано с образованием на поверхности металла тонкой, но очень плотной оксидной пленки, которая и защищает металл. По этой причине азотную и концентрированную серную кислоты транспортируют в железных емкостях.
Если металл проявляет переменные степени окисления, то с кислотами, являющимися
окислителями за счет ионов Н + , он образует соли, в которых его
степень окисления ниже устойчивой, а с кислотами-окислителями — соли, в которых
его степень окисления более устойчива:
0 +2
F
е+Н 2
SO
4
=
F
е
SO
4
+Н 2
0 разб. +
3
F
е+Н 2
SO
4
=
F
е 2 (SO 4
) 3 + 3
SO 2
+ 6Н 2
O
конц
И.И.Новошинский
Н.С.Новошинская
ОТНОШЕНИЕ МЕТАЛЛОВ К КИСЛОТАМ
Чаще всего в химической практике используются такие сильные кислоты как серная H 2 SO 4 , соляная HCl и азотная HNO 3 . Далее рассмотрим отношение различных металлов к перечисленным кислотам.
Соляная кислота ( HCl )
Соляная кислота – это техническое название хлороводородной кислоты. Получают ее путем растворения в воде газообразного хлороводорода – HCl . Ввиду невысокой его растворимости в воде, концентрация соляной кислоты при обычных условиях не превышает 38%. Поэтому независимо от концентрации соляной кислоты процесс диссоциации ее молекул в водном растворе протекает активно:
HCl H + + Cl -
Образующиеся в этом процессе ионы водорода H + выполняют роль окислителя , окисляя металлы, расположенные в ряду активности левее водорода . Взаимодействие протекает по схеме:
Me + HCl соль + H 2
При этом соль представляет собой хлорид металла (NiCl 2 , CaCl 2 , AlCl 3 ), в котором число хлорид-ионов соответствует степени окисления металла.
Соляная кислота является слабым окислителем, поэтому металлы с переменной валентностью окисляются ей до низших положительных степеней окисления :
Fe 0 → Fe 2+
Co 0 → Co 2+
Ni 0 → Ni 2+
Cr 0 → Cr 2+
Mn 0 → Mn 2+ и др .
Пример:
2 Al + 6 HCl → 2 AlCl 3 + 3 H 2
2│ Al 0 – 3 e - → Al 3+ - окисление
3│2 H + + 2 e - → H 2 – восстановление
Соляная кислота пассивирует свинец ( Pb ). Пассивация свинца обусловлена образованием на его поверхности трудно растворимого в воде хлорида свинца (II ), который защищает металл от дальнейшего воздействия кислоты:
Pb + 2 HCl → PbCl 2 ↓ + H 2
Серная кислота ( H 2 SO 4 )
В промышленности получают серную кислоту очень высокой концентрации (до 98%). Следует учитывать различие окислительных свойств разбавленного раствора и концентрированной серной кислоты по отношению к металлам.
Разбавленная серная кислота
В разбавленном водном растворе серной кислоты большинство ее молекул диссоциируют:
H 2 SO 4 H + + HSO 4 -
HSO 4 - H + + SO 4 2-
Образующиеся ионы Н + выполняют функцию окислителя .
Как и соляная кислота, разбавленный раствор серной кислоты взаимодействует только с металлами активными и средней активности (расположенными в ряду активности до водорода).
Химическая реакция протекает по схеме:
Ме + H 2 SO 4( разб .) → соль + H 2
Пример :
2 Al + 3 H 2 SO 4( разб .) → Al 2 (SO 4) 3 + 3 H 2
1│2Al 0 – 6e - → 2Al 3+ - окисление
3│2 H + + 2 e - → H 2 – восстановление
Металлы с переменной валентностью окисляются разбавленным раствором серной кислоты до низших положительных степеней окисления :
Fe 0 → Fe 2+
Co 0 → Co 2+
Ni 0 → Ni 2+
Cr 0 → Cr 2+
Mn 0 → Mn 2+ и др .
Свинец ( Pb ) не растворяется в серной кислоте (если ее концентрация ниже 80%) , так как образующаяся соль PbSO 4 нерастворима и создает на поверхности металла защитную пленку.
Концентрированная серная кислота
В концентрированном растворе серной кислоты (выше 68%) большинство молекул находятся в недиссоциированном состоянии, поэтому функцию окислителя выполняет сера , находящаяся в высшей степени окисления (S +6 ). Концентрированная H 2 SO 4 окисляет все металлы, стандартный электродный потенциал которых меньше потенциала окислителя – сульфат-иона SO 4 2- (0,36 В). В связи с этим, с концентрированной серной кислотой реагируют и некоторые малоактивные металлы .
Процесс взаимодействия металлов с концентрированной серной кислотой в большинстве случаев протекает по схеме:
Me + H 2 SO 4 (конц.) соль + вода + продукт восстановления H 2 SO 4
Продуктами восстановления серной кислоты могут быть следующие соединения серы:

Практика показала, что при взаимодействии металла с концентрированной серной кислотой выделяется смесь продуктов восстановления, состоящая из H 2 S , S и SO 2. Однако, один из этих продуктов образуется в преобладающем количестве. Природа основного продукта определяется активностью металла : чем выше активность, тем глубже процесс восстановления серы в серной кислоте.
Взаимодействие металлов различной активности с концентрированной серной кислотой можно представить схемой:

Алюминий (Al ) и железо (Fe ) не реагируют с холодной концентрированной H 2 SO 4 , покрываясь плотными оксидными пленками, однако при нагревании реакция протекает.
Ag , Au , Ru , Os , Rh , Ir , Pt не реагируют с серной кислотой.
Концентрированная серная кислота является сильным окислителем , поэтому при взаимодействии с ней металлов, обладающих переменной валентностью, последние окисляются до более высоких степеней окисления , чем в случае с разбавленным раствором кислоты:
Fe 0 → Fe 3+ ,
Cr 0 → Cr 3+ ,
Mn 0 → Mn 4+ ,
Sn 0 → Sn 4+
Свинец ( Pb ) окисляется до двухвалентного состояния с образованием растворимого гидросульфата свинца Pb ( HSO 4 ) 2 .
Примеры:
Активный металл
8 A1 + 15 H 2 SO 4( конц .) →4A1 2 (SO 4) 3 + 12H 2 O + 3H 2 S
4│2 Al 0 – 6 e - → 2 Al 3+ - окисление
3│ S 6+ + 8 e → S 2- – восстановление
Металл средней активности
2 Cr + 4 H 2 SO 4(конц.) → Cr 2 (SO 4) 3 + 4 H 2 O + S
1│ 2Cr 0 – 6e →2Cr 3+ - окисление
1│ S 6+ + 6 e → S 0 - восстановление
Металл малоактивный
2Bi + 6H 2 SO 4( конц .) → Bi 2 (SO 4) 3 + 6H 2 O + 3SO 2
1│ 2Bi 0 – 6e → 2Bi 3+ – окисление
3│ S 6+ + 2 e → S 4+ - восстановление
Азотная кислота ( HNO 3 )
Особенностью азотной кислоты является то, что азот, входящий в состав NO 3 - имеет высшую степень окисления +5 и поэтому обладает сильными окислительными свойствами. Максимальное значение электродного потенциала для нитрат-иона равно 0,96 В, поэтому азотная кислота – более сильный окислитель, чем серная. Роль окислителя в реакциях взаимодействия металлов с азотной кислотой выполняет N 5+ . Следовательно, водород H 2 никогда не выделяется при взаимодействии металлов с азотной кислотой (независимо от концентрации ). Процесс протекает по схеме:
Me + HNO 3 соль + вода + продукт восстановления HNO 3
Продукты восстановления HNO 3 :
Обычно при взаимодействии азотной кислоты с металлом образуется смесь продуктов восстановления, но как правило, один из них является преобладающим. Какой из продуктов будет основным, зависит от концентрации кислоты и активности металла.
Концентрированная азотная кислота
Концентрированным считают раствор кислоты плотностью
ρ > 1,25 кг/м 3 , что соответствует
концентрации > 40%. Независимо от активности металла реакция взаимодействия
с
HNO
3 (конц.)
протекает
по схеме:
Me + HNO 3 (конц.) → соль + вода + NO 2
С концентрированной азотной кислотой не взаимодействуют благородные металлы (Au , Ru , Os , Rh , Ir , Pt ), а ряд металлов (Al , Ti , Cr , Fe , Co , Ni ) при низкой температуре пассивируются концентрированной азотной кислотой. Реакция возможна при повышении температуры, она протекает по схеме, представленной выше.
Примеры
Активный металл
Al + 6 HNO 3( конц .) → Al (NO 3 ) 3 + 3 H 2 O + 3 NO 2
1│ Al 0 – 3 e → Al 3+ - окисление
3│ N 5+ + e → N 4+ - восстановление
Металл средней активности
Fe + 6 HNO 3(конц.) → Fe(NO 3) 3 + 3H 2 O + 3NO
1│ Fe 0 – 3e → Fe 3+ - окисление
3│ N 5+ + e → N 4+ - восстановление
Металл малоактивный
Ag + 2HNO 3( конц .) → AgNO 3 + H 2 O + NO 2
1│ Ag 0 – e → Ag + - окисление
1│ N 5+ + e → N 4+ - восстановление
Разбавленная азотная кислота
Продукт восстановления азотной кислоты в разбавленном растворе зависит от активности металла , участвующего в реакции:

Примеры:
Активный металл
8 Al + 30 HNO 3(разб.) → 8Al(NO 3) 3 + 9H 2 O + 3NH 4 NO 3
8│ Al 0 – 3e → Al 3+ - окисление
3│ N 5+ + 8 e → N 3- - восстановление
Выделяющийся в процессе восстановления азотной кислоты аммиак сразу взаимодействует с избытком азотной кислоты, образуя соль – нитрат аммония NH 4 NO 3 :
NH 3 + HNO 3 → NH 4 NO 3.
Металл средней активности
10Cr + 36HNO 3( разб .) → 10Cr(NO 3) 3 + 18H 2 O + 3N 2
10│ Cr 0 – 3 e → Cr 3+ - окисление
3│ 2 N 5+ + 10 e → N 2 0 - восстановление
Кроме молекулярного азота (N 2 ) при взаимодействии металлов средней активности с разбавленной азотной кислотой образуется в равном количестве оксид азота (I ) – N 2 O . В уравнении реакции нужно писать одно из этих веществ .
Металл малоактивный
3Ag + 4HNO 3( разб .) → 3AgNO 3 + 2H 2 O + NO
3│ Ag 0 – e → Ag + - окисление
1│ N 5+ + 3 e → N 2+ - восстановление
«Царская водка»
«Царская водка» (ранее кислоты называли водками) представляет собой смесь одного объема азотной кислоты и трех-четырех объемов концентрированной соляной кислоты, обладающую очень высокой окислительной активностью. Такая смесь способна растворять некоторые малоактивные металлы, не взаимодействующие с азотной кислотой. Среди них и «царь металлов» - золото. Такое действие «царской водки» объясняется тем, что азотная кислота окисляет соляную с выделением свободного хлора и образованием хлороксида азота (III ), или хлорида нитрозила – NOCl :
HNO 3 + 3 HCl → Cl 2 + 2 H 2 O + NOCl
2 NOCl → 2 NO + Cl 2
Хлор в момент выделения состоит из атомов. Атомарный хлор является сильнейшим окислителем, что и позволяет «царской водке» воздействовать даже на самые инертные «благородные металлы».
Реакции окисления золота и платины протекают согласно следующим уравнениям:
Au + HNO 3 + 4 HCl → H + NO + 2H 2 O
3Pt + 4HNO 3 + 18HCl → 3H 2 + 4NO + 8H 2 O
На Ru , Os , Rh и Ir «царская водка» не действует.
Е.А. Нуднoва, М.В. Андрюxова
Соли-продукт замещения атомов водорода в кислоте на металл. Растворимые соли в соде диссоцируют на катион металла и анион кислотного остатка. Соли делят на:
· Средние
· Основные
· Комплексные
· Двойные
· Смешанные
Средние соли. Это продукты полного замещения атомов водорода в кислоте на атомы металла, или на группу атомов (NH 4 +): MgSO 4 ,Na 2 SO 4 ,NH 4 Cl, Al 2 (SO 4) 3 .
Названия средних солей происходят от названия металлов и кислот:CuSO 4 -сульфат меди,Na 3 PO 4 -фосфат натрия,NaNO 2 -нитрит натрия,NaClO-гипохлорит натрия,NaClO 2 -хлорит натрия,NaClO 3 -хлорат натрия,NaClO 4 -перхлорат натрия,CuI- йодид меди(I), CaF 2 -фторид кальция. Так же надо запомнить несколько тривиальных названий: NaCl-поваренная соль, KNO3-калийная селитра, K2CO3-поташ, Na2CO3-сода кальцинированная,Na2CO3∙10H2O-сода кристаллическая, CuSO4- медный купорос,Na 2 B 4 O 7 . 10H 2 O- бура,Na 2 SO 4 . 10H 2 O-глауберова соль.Двойные соли. Это соли, содержащие два типа катионов (атомы водорода многоосновной кислоты замещены двумя различными катионами): MgNH 4 PO 4 , KAl (SO 4 ) 2 , NaKSO 4 .Двойные соли как индивидуальные соединения существуют только в кристаллическом виде. При растворении в воде они полностью диссоциируютна ионы металлов и кислотные остатки (если соли растворимые), например:
NaKSO 4 ↔ Na + + K + + SO 4 2-
Примечательно, что диссоциация двойных солей в водных растворах проходит в 1 ступень. Для названия солей данного типа нужно знать названия аниона и двух катионов: MgNH 4 PO 4 - фосфат магния-аммония.
Комплексные соли. Это частицы (нейтральные молекулы или ионы), которые образуются в результате присоединения к данному иону(или атому), называемомукомплексообразователем , нейтральных молекул или других ионов, называемых лигандами . Комплексные соли делятся на:
1) Катионные комплексы
Cl 2 - дихлоридтетраамминцинка(II)
Cl 2 -
ди
хлоридгексаамминкобальта(II)
2) Анионные комплексы
K 2 -
тетрафторобериллат(II) калия
Li -
тетрагидридоалюминат(III) лития
K 3 -
гексацианоферрат(III) калия
Теорию строения комплексных соединений разработал швейцарский химик А. Вернер.
Кислые соли – продукты неполного замещения атомов водорода в многоосновных кислотах на катионы металла.
Например: NaHCO 3
Химические свойства:
Реагируют с металлами, стоящими в ряду напряжений левее водорода
.
2KHSO 4 +Mg→H 2 +Mg(SO) 4 +K 2
(SO) 4
Заметим, что для таких реакций опасно брать щелочные металлы, ибо они вначале прореагируют с водой с большим выделением энергии, и произойдёт взрыв, так как все реакции происходят в растворах.
2NaHCO 3 +Fe→H 2 +Na 2 CO 3 +Fe 2 (CO 3) 3 ↓
Кислые соли реагируют с растворами щелочей и образуют среднюю(ие) соль(ли) и воду:
NaHCO 3 +NaOH→Na 2 CO 3 +H 2 O
2KHSO 4 +2NaOH→2H 2 O+K 2 SO 4 +Na 2 SO 4
Кислые соли реагируют с растворами средних солей в том случае, если выделяется газ, выпадает осадок, или выделяется вода:
2KHSO 4 +MgCO 3 →MgSO 4 +K 2 SO 4 +CO 2 +H 2 O
2KHSO 4 +BaCl 2 →BaSO 4 ↓+K 2 SO 4 +2HCl
Кислые соли реагируют с кислотами, если кислота-продукт реакции будет более слабая или летучая, чем добавленная.
NaHCO 3 +HCl→NaCl+CO 2 +H 2 O
Кислые соли реагируют с основными оксидами с выделением воды и средних солей:
2NaHCO 3 +MgO→MgCO 3 ↓+Na 2 CO 3 +H 2 O
2KHSO 4 +BeO→BeSO 4 +K 2 SO 4 +H 2 O
Кислые соли (в частности гидрокарбонаты) разлагаются под действием температуры:
2NaHCO 3 → Na 2
CO 3 +CO 2 +H 2 O
Получение:
Кислые соли образуются при воздействии на щёлочь избытком раствора многоосновной кислоты (реакция нейтрализации):
NaOH+H 2 SO 4 →NaHSO 4 +H 2 O
Mg(OH) 2 +2H 2 SO 4 →Mg(HSO 4) 2 +2H 2 O
Кислые соли образуются при растворении основных оксидов в многоосновных кислотах:
MgO+2H 2 SO 4 →Mg(HSO 4) 2 +H 2 O
Кислые соли образуются при растворении металлов в избытке раствора многоосновной кислоты:
Mg+2H 2 SO 4 →Mg(HSO 4) 2 +H 2
Кислые соли образуются в результате взаимодействия средней соли и кислоты, которой образован анион средней соли:
Ca 3 (PO 4) 2 +H 3 PO 4 →3CaHPO 4
Основные соли:
Основные соли – продукт неполного замещения гидроксогруппы в молекулах многокислотных оснований на кислотные остатки .
Пример: MgOHNO 3 ,FeOHCl.
Химические свойства:
Основные соли реагируют с избытком кислоты, образуя среднюю соль и воду.
MgOHNO 3 +HNO 3 →Mg(NO 3) 2 +H 2 O
Основные соли разлагаются температурой:
2 CO 3 →2CuO+CO 2 +H 2 O
Получение основных солей:
Взаимодействие солей слабых кислот со средними солями:
2MgCl 2 +2Na 2 CO 3 +H 2 O→ 2
CO 3 +CO 2 +4NaCl
Гидролиз солей, образованных слабым основанием и сильной кислотой:
ZnCl 2 +H 2 O→Cl+HCl
Большинство основных солей являются малорастворимыми. Многие из них являются минералами, напримермалахит Cu 2 CO 3 (OH) 2 и гидроксилапатит Ca 5 (PO 4) 3 OH.
Свойства смешанных солей не рассматриваются в школьном курсе химии, но определение важно знать.
Смешанные соли – это соли, в составе которых к одному катиону металла присоединены кислотные остатки двух разных кислот.
Наглядный пример -Ca(OCl)Cl белильная известь (хлорка).
Номенклатура:
1. Соль содержит комплексный катион
Сначала называют катион, затем входящие в внутреннюю сферу лиганды- анионы, с окончанием на «о» (Cl - - хлоро, OH - -гидроксо), затем лиганды, представляющие собой нейтральные молекулы (NH 3 -амин, H 2 O -акво).Если одинаковых лигандов больше 1, о их количество обозначают греческими числительными: 1 - моно, 2 - ди,3 - три, 4 - тетра, 5 - пента, 6 - гекса, 7 - гепта, 8 - окта, 9 - нона, 10 - дека. Последним называют ион-комплексообразователь, в скобках указывая его валентность, если она переменная.
[ Ag (NH 3 ) 2 ](OH )-гидроксид диамин серебра (I )
[ Co (NH 3 ) 4 Cl 2 ] Cl 2 -хлорид дихлор o тетраамин кобальта (III )
2. Соль содержит комплексный анион.
Сначала называют лиганды -анионы, затем входящие в внутреннюю сферу нейтральные молекулы с окончанием на «о», указывая их количество греческими числительными. Последним называют ион-комплексообразователь на латинском, с суффиксом «ат», указывая в скобочках валентность. Далее пишется название катиона, находящегося в внешней сфере, число катионов не указывается.
K 4 -гексацианоферрат (II) калия(реактив на ионы Fe 3+)
K 3 - гексацианоферрат (III) калия(реактив на ионы Fe 2+)
Na 2 -тетрагидроксоцинкат натрия
Большинство ионов комплексообразователей- металлы. Наибольшую склонность к комплексообрзованию проявляют d элементы. Вокруг центрального иона-комплексообразователя находятся противоположно заряженные ионы или нейтральные молекулы- лиганды или адденды.
Ион-комплексообразователь и лиганды составляют внутреннюю сферу комплекса (в квадратных скобочках), число лигандов, координирующихся вокруг центрального иона называют координационным числом.
Ионы, не вошедшие в внутреннюю сферу, образуют внешнюю сферу. Если комплексный ион- катион, то во внешней сфере анионы и наоборот, если комплексный ион-анион, то во внешней сфере- катионы. Катионами обычно являются ионы щелочных и щёлочноземельных металлов, катион аммония. При диссоциации комплексные соединения дают сложные комплексные ионы, которые довольно устойчивы в растворах:
K 3 ↔3K + + 3-
Если речь идёт о кислых солях, то при чтении формулы произносится приставка гидро-, например:
Гидросульфид натрия NaHS
Гидрокарбонат натрия NaHCO 3
С основными солями же используется приставка гидроксо- или дигидроксо-
(зависит от степени окисления металла в соли), например:
гидроксохлорид магнияMg(OH)Cl, дигидроксохлорид алюминия Al(OH) 2 Cl
Способы получения солей:
1. Прямое взаимодействие металла с неметаллом . Этим способом можно получают соли бескислородных кислот.
Zn+Cl 2 →ZnCl 2
2. Взаимодействие кислоты и основания (реакция нейтрализации). Реакции этого типа имеют большое практическое значение (качественные реакции на большинство катионов), они всегда сопровождаются выделением воды:
NaOH+HCl→NaCl+H 2 O
Ba(OH) 2 +H 2 SO 4 →BaSO 4 ↓+2H 2 O
3. Взаимодействие основного оксида с кислотным :
SO 3 +BaO→BaSO 4 ↓
4. Взаимодействие кислотного оксида и основания :
2NaOH+2NO 2 →NaNO 3 +NaNO 2 +H 2 O
NaOH+CO 2 →Na 2 CO 3 +H 2 O
5. Взаимодействие основного оксида и кислота :
Na 2 O+2HCl→2NaCl+H 2 O
CuO+2HNO 3 =Cu(NO 3) 2 +H 2 O
6. Прямое взаимодействие металла с кислотой. Эта реакция может сопровождаться выделением водорода. Будет ли выделяться водорода или нет зависит от активности металла, химических свойств кислоты и ее концентрации (см. Свойства концентрированной серной и азотной кислот).
Zn+2HCl=ZnCl 2 +H 2
H 2 SO 4 +Zn=ZnSO 4 +H 2
7. Взаимодействие соли с кислотой . Эта реакция будет происходить при условии, что кислота, образующая соль слабее или более летуча, чем кислота, вступившая в реакцию:
Na 2 CO 3 +2HNO 3 =2NaNO 3 +CO 2 +H 2 O
8. Взаимодействие соли с кислотным оксидом. Реакции идут только при нагревании, поэтому, вступающий в реакцию оксид должен быть менее летучим, чем образующийся после реакции:
CaCO 3 +SiO 2 =CaSiO 3 +CO 2
9. Взаимодействие неметалла с щелочью . Галогены, сера и некоторые другие элементы, взаимодействуя с щелочами дают бескислородную и кислородосодержащую соли:
Cl 2 +2KOH=KCl+KClO+H 2 O(реакция идёт без нагревания)
Cl 2 +6KOH=5KCl+KClO 3 +3H 2 O (реакция идёт с нагреванием)
3S+6NaOH=2Na 2 S+Na 2 SO 3 +3H 2 O
10. Взаимодействие между двумя солями. Это наиболее распространённыйспособ получения солей. Для этого обе соли, вступившие в реакцию должны бать хорошо растворимы, а так как это реакция ионного обмена, то, для того, чтобы она прошла до конца, нужно чтобы 1 из продуктов реакции был нерастворим:
Na 2 CO 3 +CaCl 2 =2NaCl+CaCO 3 ↓
Na 2 SO 4 + BaCl 2 =2NaCl+BaSO 4 ↓
11. Взаимодействие между солью и металлом . Реакция протекает в том случае, если металл стоит в ряду напряжения металлов левее того, который содержится в соли:
Zn+CuSO 4 =ZnSO 4 +Cu↓
12. Термическое разложение солей . При нагревании некоторых кислородосодержащих солей образуются новые, с меньшим содержанием кислорода, или вообще его не содержащие:
2KNO 3 → 2KNO 2 +O 2
4KClO 3 → 3KClO 4 +KCl
2KClO 3 → 3O 2 +2KCl
13. Взаимодействие неметалла с солью. Некоторые неметаллы способны соединяться с солями, с образованием новых солей:
Cl 2 +2KI=2KCl+I 2 ↓
14. Взаимодействие основания с солью . Так как это реакцияионного обмена, то, для того, чтобы она прошла до конца, нужно чтобы 1 из продуктов реакции был нерастворим (это реакция так же пользуются для перевода кислых солей в средние):
FeCl 3 +3NaOH=Fe(OH) 3 ↓ +3NaCl
NaOH+ZnCl 2 = (ZnOH)Cl+NaCl
KHSO 4 +KOH=K 2 SO 4 +H 2 O
Так же таким способом можно получать и двойные соли:
NaOH+ KHSO 4 =KNaSO 4 +H 2 O
15. Взаимодействие металла с щелочью. Металлы, которые являются амфотерными реагируют с щелочами, образуя комплексы:
2Al+2NaOH+6H 2 O=2Na+3H 2
16. Взаимодействие солей(оксидов, гидроксидов, металлов) с лигандами:
2Al+2NaOH+6H 2 O=2Na+3H 2
AgCl+3NH 4 OH=OH+NH 4 Cl+2H 2 O
3K 4 +4FeCl 3 =Fe 3 3 +12KCl
AgCl+2NH 4 OH=Cl+2H 2 O
Редактор: Харламова Галина Николаевна